“手搓”疫苗,把癌症治好了?


独家抢先看
如今的罗茜,能在院子里跑,能追兔子,能叼着玩具和大家玩。几个月前,这只8岁的混血犬因腿部肿瘤恶化虚弱不堪,医生判断它可能只剩下几个月生命。
最近,这只狗和其主人的故事突然出圈。它的主人保罗·康宁汉姆是一名澳大利亚的程序员,借助AI大模型和当地科学家的帮助,为罗茜设计了一套个性化治疗方案,其中包括一款定制mRNA癌症疫苗。报道称,治疗后不到两个月,罗茜部分肿瘤缩小了75%。OpenAI联合创始人兼总裁格雷格·布罗克曼在社交媒体上称,这是“透视通用人工智能机遇的一个小窗口”。
不过,这一故事收获广泛赞誉的同时,也在科研圈引发质疑:一个没有任何医学背景的人,借助几款大语言模型设计出的癌症治疗方案,真的靠谱吗?这种方式是否能推广到癌症患者身上?
图片来源:保罗·康宁汉姆
“并未被治愈”
康宁汉姆是澳大利亚一家AI初创公司的创始人。2019年,他领养了罗茜。五年后,罗茜被诊断出患有肥大细胞癌,这是一种犬类较常见的皮肤癌。在确诊前很长一段时间,罗茜腿部的异常一直被当作普通皮疹处理,其病情不断加重。
为了治疗罗茜的癌症,康宁汉姆花费数千美元为爱犬进行化疗、手术,虽减缓了病情,但肿瘤并未缩小。拥有近二十年机器学习和数据分析经验的康宁汉姆决定向AI求助。
“坦白说,最初我对癌症几乎一无所知。”康宁汉姆在近期的一次播客中回忆,但他一直关注AI在药物设计领域的进展。于是,他打开ChatGPT,系统梳理癌症治疗的逻辑和不同方案的作用机制,同时,他开始真正理解免疫治疗的核心:调动身体自身的免疫系统去对抗癌症。
ChatGPT给出的第一步建议,是对罗茜的肿瘤和血液样本进行基因测序。康宁汉姆联系了澳大利亚新南威尔士大学的一家基因组学中心,获得罗茜的健康细胞和肿瘤组织的基因组数据。
癌细胞和正常细胞不同,是因为其携带的某些基因发生了突变,这可以视作癌细胞的“指纹”或“身份证”。这些突变可能会产生异常蛋白,或异常蛋白片段。mRNA癌症疫苗要做的,就是把这些异常特征提前“告诉”免疫系统,帮助身体更早识别并攻击癌细胞。
通过比对,康宁汉姆锁定了与罗茜癌症关联密切的异常蛋白。康宁汉姆使用AlphaFold为这种蛋白生成了三维模型,以便在计算机上模拟药物与蛋白的相互作用。AlphaFold是谷歌DeepMind开发的蛋白质结构预测工具。然而,无论是尝试设计新药,还是筛选已有药物分子,均以失败告终。
转机来自一次散步。2025年7月的一天,康宁汉姆带着罗茜出门,走着走着脑子里突然冒出一个念头:基于他已完成的一些工作,或许已走在为罗茜开发免疫疗法的路上了。
回家后,他把之前所有工作整理了一遍输给ChatGPT,并提问:这些能不能转化成一种免疫治疗方案?ChatGPT明确回答“可以”,并表示康宁汉姆已非常接近做出一种新抗原肽疫苗或mRNA疫苗。
随后,康宁汉姆联系了新南威尔士大学的学者。在专家帮助下,他重新分析了罗茜癌细胞的所有突变,筛选出最有可能被免疫系统识别的“指纹”。之后,他利用Gemini和Grok等AI大模型验证,得到一段构建疫苗的序列。两个月内,科学家团队根据这段序列,为罗茜定制了一款mRNA疫苗。
这支疫苗并不是罗茜接受的全部治疗。按照康宁汉姆的设计,罗茜接受的是一套联合方案,除了mRNA疫苗,还包括PD-1和酪氨酸激酶抑制剂。也就是说,罗茜肿瘤的变化,并不能简单理解为“只靠一支疫苗”。
在3个月的伦理审批后,去年12月,罗茜接受了第一针注射,今年2月后又打了后续针剂。康宁汉姆谈道,注射后的前两周,罗茜的肿瘤反而变大了。他认为,这种肿胀在免疫疗法里,通常是个好迹象,意味着免疫细胞正大量聚集到癌症病灶处。今年1月之后,他注意到,核桃大小的肿胀开始消退,部分肿瘤开始缩小。
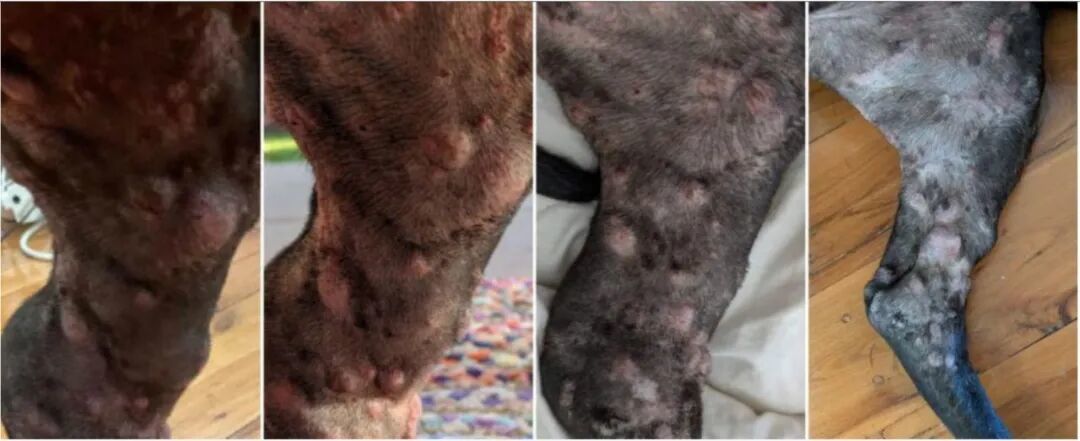
罗茜的肿瘤逐渐缩小,从左至右:1. 2025年11月,试验开始前。2. 2025年12月,mRNA注射后一周。3. 2026年1月,试验进行七周后。4. 2026年3月。来源:《澳大利亚人报》
不过,康宁汉姆强调,罗茜并未被治愈,这只是为罗茜带来更好的生活质量。据《澳大利亚人报》报道,即便经历这一切之后,康宁汉姆认为罗茜仍可能只剩几个月的生命。康宁汉姆并未放弃。新南威尔士大学正对罗茜体内一个未对治疗产生反应的肿瘤样本进行测序。
“更像是一个吸引眼球的个案”
故事传开后,质疑声随之而来。
原因在于很大程度上它带有一种强烈的“工程师借助AI单枪匹马搞定一切”的叙事色彩。但很快有声音指出,AI在其中的作用被放大了。在这一过程中,ChatGPT、AlphaFold等更像是帮助人类理解复杂信息的辅助系统,而非癌症治疗方案的真正创造者。
“这更像是一个吸引眼球的个案,而不是科学上的新发现。”清华大学药学院创始院长丁胜在接受《中国新闻周刊》采访时直言,肿瘤测序、突变比对等环节,在AI热潮到来之前就已存在。在他看来,康宁汉姆所做的事,即便没有ChatGPT,同样可以完成,AI只是更加有效地让非专业领域的人尝试整个流程,但对癌症治疗还谈不上带来范式转变。
图片来源:保罗·康宁汉姆
公众更关心的是:未来是否真的可能“靠AI在家‘手搓’出个性化癌症疫苗”?对此,多位受访专家的回答都很明确:这离实现仍十分遥远。
在医学领域,决定一项技术价值的是大样本、可重复、可验证的临床结果。丁胜并不推荐把康宁汉姆的做法当成一种可复制模式。他谈道,类似“肿瘤缩小”的个案,在动物实验和临床研究中都不罕见。而判断一种治疗方式是否真的有效,关键要看它在一定人群内,对比安慰剂是否有统计学意义,能不能在不同阶段的临床研究中稳定体现出优势。
罗茜的治疗过程本身也缺乏对照,这也是争议之一。康宁汉姆的方案同时包含mRNA疫苗、PD-1抑制剂和酪氨酸激酶抑制剂。肿瘤缩小,多大程度归功于疫苗本身,是联合治疗的叠加效果,还是其他成熟药物贡献了主要疗效,目前都无法判断。
丁胜分析,治疗中叠加的药物越多,对照设计就越复杂,并且,理论上完全存在一种可能:即便不使用这支mRNA疫苗,治疗效果也未必更差。mRNA癌症疫苗整体仍处于早期探索阶段,距离真正成熟并广泛应用于临床,还有很长的路要走。
他进一步解释,个性化癌症疫苗的核心,是根据每个患者肿瘤的异常特征“量身定制”治疗。但不同癌症对这类治疗的反应并不一样,实体瘤和血液瘤差别就很大。即便是同一种癌症,不同患者的免疫状态、肿瘤特征和个体差异也很明显。所以从概念上看,它有希望发展成一种通用方法;但在实际操作中,它仍是一个高度复杂的问题。
清华大学药学院副院长尹航在接受《中国新闻周刊》采访时谈道,mRNA癌症疫苗真正的难点,是怎么证明它对人有效、安全,并且适用于不同年龄、不同基础疾病和不同治疗阶段的人群。
此外,尹航表示,AI在制药中的价值是真实存在的,在靶点发现、结构预测等环节能明显提升效率,但它并不是一种“万能设计器”。现阶段,AI最擅长的,仍是在训练数据足够丰富、评价标准较明确的场景中发挥作用,它能走多远,关键取决于输入的数据质量。问题在于,真实临床情况非常复杂,目前仍缺少足够多“AI设计的药物进入人体后效果如何”的高质量数据。
尹航称,在癌症疫苗领域,安全性这一关AI还远未跨过。目前,这一领域的很多训练数据主要来自细胞实验、动物模型等,这些当然有参考价值。但动物实验有效,不代表对人体有效;模型里看起来安全,也不等于真实使用时就没有风险。
当然,这并不意味着个性化癌症疫苗不值得关注。今年1月,莫德纳与默沙东合作开发的一款个性化mRNA癌症疫苗,在一项针对高危黑色素瘤患者的Ⅱ期研究中,将复发或死亡风险降低了49%。丁胜也提到,如今有不少公司在推进相关研发,只是大多数项目仍处在早期探索阶段。
多位受访专家指出,未来癌症治疗大概率仍将沿着联合用药的方向发展。即便将来真正成熟,个性化疫苗也更可能成为整体治疗方案中的一个组成部分,而不是“单兵作战”。
尹航认为,这一故事说明,AI、mRNA和个体化治疗的结合,已开始从实验室走向现实。未来,在保障安全性的前提下,AI很可能贯穿药物设计、评价、优化等多个环节,成为重要工具,但真正走到临床应用,还要跨过技术、伦理、监管、质量控制和长期随访等多重门槛。
记者:牛荷
编辑:杜玮
运营编辑:王琳
“特别声明:以上作品内容(包括在内的视频、图片或音频)为凤凰网旗下自媒体平台“大风号”用户上传并发布,本平台仅提供信息存储空间服务。
Notice: The content above (including the videos, pictures and audios if any) is uploaded and posted by the user of Dafeng Hao, which is a social media platform and merely provides information storage space services.”